Acid oksalik
Agjencia Federale për Arsimin
Institucion arsimor shtetëror i arsimit të lartë profesional
UNIVERSITETI TEKNIK SHTETROR VOLGOGRAD
(VolgSTU)
Departamenti "Teknologjia e peshave të larta molekulare dhe materialeve fibroze"
Punë semestrale
në disiplinën "Bazat e proceseve kimike"
Tema: “Karakteristikat e proceseve që ndodhin gjatë sintezës së acidit oksalik. Llogaritja e bilancit të materialit dhe nxehtësisë ".
Volgograd 2011
Karakteristikat kimike.
Karakteristikat fizike.
Metodat e marrjes.
Aplikacion
Tregu i shitjeve
GOST për shitje
Bilanci material
Bilanci i nxehtësisë
Karakteristikat kimike:
Acidi oksalik (acid etanedioik) C 2 H 2 O 4 është një acid karboksilik i ngopur dibazik. Bën pjesë në acide të forta organike. Ka të gjitha vetitë kimike të acideve karboksilike. Kripërat dhe esteret e acidit oksalik quhen oksalate. Gjendet natyrshëm në lëpjetë dhe disa bimë të tjera në formën e oksalateve të kaliumit dhe kalciumit.
Acidi oksalik u sintetizua për herë të parë në 1842 nga kimisti gjerman Friedrich Wöhler nga cianogjeni. Acidi oksalik (ose joni oksalat C 2 O 4 2-) është një agjent reduktues (çngjyros tretësirën e KMnO4).
Acidi oksalik është lehtësisht i tretshëm në ujë dhe alkool. Isshtë një acid organik relativisht i fortë (klasa e rrezikut 3), HOOC-COOH, është një kristal higroskopik pa ngjyrë, i tretshëm lehtësisht në ujë, i kufizuar në alkool etilik dhe eter dietil, i patretshëm në kloroform, eter nafte dhe benzinë. Formon një dihidrat të përbërjes C 2 H 2 O 4 * 2H 2 O. Një substancë e djegshme, në një gjendje të vendosur është e rrezikshme nga zjarri. Ka një efekt irritues të fortë në lëkurë, mukozën e syve dhe traktin e sipërm respirator.
Acidi oksalik ka vetitë kimikekarakteristikë e acideve karboksilike, duke formuar dy seri derivatesh. Kripërat dhe esteret e acidit oksalik quhen oksalate. Acidi oksalik formon estere acide dhe të mesme, amide, klorid acid.
Acidi oksalik gjendet në lëpjetë dhe raven si oksalat kaliumi.

Ky acid është shumë i përhapur në botën bimore - gjendet në formën e kripërave në gjethet e lëpjetë, të thartë, raven, etj. Kripërat dhe esteret e këtij acidi kanë një emër të parëndësishëm - oksalate (nga greqishtja "oxalis" - lëpjetë).
shfaq vetitë e përgjithshme të acideve, njësoj. pasi ka një grup funksional karboksil. Reaksioni i formimit të kripës provon vetitë acidike të acidit formik. Në këtë rast, kripërat formohen - formate.
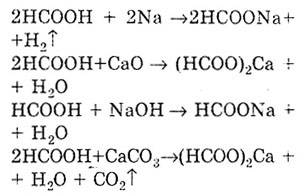
Si të gjithë acidet karboksilike, acidi formik formon esteret.
Reagimi i esterifikimit:
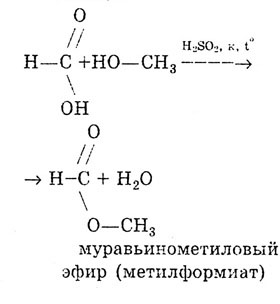
Acidi formik ndryshon nga acidet e tjerë karboksilikë në atë që grupi karboksil në të nuk është i lidhur me një radikal hidrokarbure, por me një atom hidrogjeni. Prandaj, acidi formik mund të konsiderohet si një acid dhe një aldehid:

Ashtu si aldehidet, acidi formik mund të oksidohet:
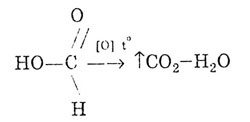
Acidi formik jep një reagim pasqyre argjendi:
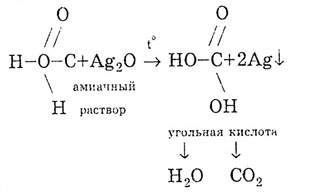
Acidi formik zbërthehet kur nxehet:
![]()
acidi formik bën pjesë në serinë homologe të acideve karboksilike monobazike
Karakteristikat fizike:
Temperatura e lartësimit: shih shënimet ° C
Pika e shkrirjes: 102 ° C
Dendësia relative (ujë \u003d 1): 1.7
Tretshmëria në ujë, g / 100 ml: 10
Presioni i avullit në Pa në 30 ° C: shih Shënimet
Dendësia relative e avullit (ajri \u003d 1): 3.1
Acidi oksalik është një nga acidet më të forta karboksilike, shumë më superior në forcë se homologët e tij.
Acidi etanedioik shfaq veti reduktuese: në një tretësirë \u200b\u200btë acidifikuar të permanganatit të kaliumit, oksidohet në monoksid karboni (IV) dhe ujë.
Kur nxehet në prani të acidit sulfurik, ndodh dekarboksilimi dhe merren monoksid karboni (IV) dhe acid formik.
Pikat e vlimit të acideve yndyrore të strukturës normale natyrshëm rriten me një rritje të numrit të atomeve të karbonit. Hasshtë zbuluar se molekulat e acidit shoqërohen në të njëjtën mënyrë siç shoqërohen molekulat e ujit ose alkoolit. Acidet e ulëta distilohen mirë me avull dhe prandaj zakonisht referohen si acide yndyrore të paqëndrueshme.
Pikat e shkrirjes së acideve monobazike gjithashtu zakonisht rriten ndërsa numri i atomeve të karbonit në molekulat e tyre rritet; por vërehet rregullsia e mëposhtme: acidet me një zinxhir normal, që kanë një numër të barabartë të atomeve të karbonit, zakonisht shkrihen në një temperaturë më të lartë se anëtarët e mëparshëm dhe të mëpasshëm të serisë homologe, të cilat kanë një numër tek të atomeve të karbonit.
RREZIKET KIMIKE:
Substanca zbërthehet në ngrohjen e shpejtë mbi rreth 150 ° C duke prodhuar gaz toksik. Tretësirë \u200b\u200buji është një acid me fuqi të mesme që reagon me dhunë me baza të forta. Reagon me dhunë me oksidantët duke shkaktuar rrezik zjarri dhe shpërthimi. Reagon me argjendin për të formuar produkte shpërthyese.
Aplikacion.
Acidi oksalik dhe kripërat e tij përdoren në industrinë e tekstilit dhe lëkurës si mordant; si një përbërës i banjove anode për depozitimin e veshjeve Al, Ti dhe Sn; si reagjent në kiminë analitike dhe organike; përbërësi i përbërjeve për pastrimin e metaleve nga ndryshku dhe oksidet; për depozitimin e elementeve të rralla të tokës. Oksamidi është një stabilizues i nitrateve të celulozës, cian është një reagues në sintezën organike, oksalil kloruri është një reagjent klorinues, klorokarbonilues dhe ndërlidhës në sintezën organike. Oksalatet e diakil, kryesisht oksalati i dietilit dhe oksalati i dibutilit, përdoren si tretës të celulozës; disa esterë të acidit oksalik dhe fenoleve të zëvendësuara - si reagjentë kimiluminescent.
Acidi oksalik përdoret për lustrimin e metaleve, në industrinë e përpunimit të drurit, në pastrimin e uraniumit
Fushat e acidit oksalik dhe kripërave të tij (oksalate):
në industrinë kimike (sinteza organike, në prodhimin e plastikës, bojës, në sintezën e ngjyrave, si përbërës i përbërjeve piroteknike);
në metalurgjinë kimike (si përbërës i përbërjeve për pastrimin e metaleve nga ndryshku, shkalla, oksidet);
në kiminë analitike (si një precipitant për elementë të rrallë të tokës);
në mikroskopi (si një agjent zbardhues për feta);
në industrinë e tekstilit dhe lëkurës (i butë në shtypjen e pambukut dhe ngjyrosjen e leshit dhe mëndafshit, lëkura për rrezitje);
në prodhimin e detergjenteve sintetikë (si zbardhues dhe dezinfektues, një mjet për pastrimin dhe largimin e gurëve urinarë, kripërave të fortësisë dhe ndryshkut);
në kozmetikë (si një shtesë aktive në zbardhjen dhe kremrat e njollave);
në sistemet e pastrimit të ujit (metoda kimike e pastrimit dhe zvogëlimit të fortësisë së ujit, pastrimi i ftohësve në termocentralet bërthamore);
në mjekësi dhe farmaceutikë.
Metodat e marrjes:
1) Si një nënprodukt në prodhimin e acidit acetik nga oksidimi në fazë të lëngët të butanit.
2) Oksidimi i metanolit:
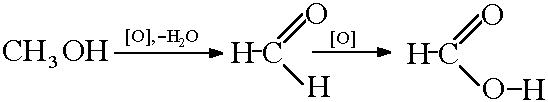
Reagimi i monoksidit të karbonit me hidroksid natriumi:
NaOH + CO → HCOONa (+ H3SO4, −Na2SO4) HCOOH
Kjo është metoda kryesore industriale, e cila kryhet në dy faza: në fazën e parë, monoksidi i karbonit nën një presion prej 0.6-0.8 MPa kalon përmes hidroksidit të natriumit të nxehtë në 120-130 ° C; në fazën e dytë, formati i natriumit trajtohet me acid sulfurik dhe produkti distilohet në vakum.
Zbërthimi i estereve të glicerinës së acidit oksalik. Për këtë, glicerina anhidrike nxehet me acid oksalik, ndërsa uji distilohet dhe formohen esteret oksalike. Me ngrohjen e mëtutjeshme, esteret zbërthehen, duke çliruar dioksid karboni dhe formohen estere formike, të cilat, pasi zbërthehen me ujë, japin acid formik dhe glicerinë.
Acidi dibasik karboksilik kufizues me formulën bruto C2H2O4 quhet, sipas nomenklaturës sistematike, acid etanedioik. Kjo substancë njihet gjithashtu me një emër tjetër, më të zakonshëm - acid oksalik. Ajo u mor për herë të parë nga kimisti gjerman F. Wöhler nga cianogjeni (acid oksalik dinitrile) në 1824. Kristalet e pangjyrë të acidit treten në ujë për të formuar tretësira pa ngjyrë. Masa molare është 90,04 g / mol. Nga pamja e jashtme i ngjan kristaleve pa ngjyra monoklinike. Në një temperaturë prej 20 ° C, 8 g acid oksalik shpërndahen në 100 g ujë. Ai tretet mirë në aceton, alkool etilik dhe eter sulfurik. Dendësia 1.36 g / cm³. Shkrihet në një temperaturë prej 189.5 ° C, sublimes në 125 ° C, dekompozohet në 100-130 ° C.
Acidi oksalik ka të gjitha vetitë kimike karakteristike të acideve karboksilike. Formula e tij është: NOOS-COOH. Përkundër faktit se i përket acideve karboksilike, ai konsiderohet një acid i fortë organik (3000 herë më i fortë se acid acetik): C2O4H2 → C2O4H- + H + (рК \u003d 1.27) dhe më tej: C2O4H- → C2O42 - + H + (рК \u003d 4.27). Esteret dhe kripërat e këtij acidi quhen oksalate. Joni oksalat C2O42− është një agjent zvogëlues. Kur acidi oksalik reagon me (KMnO4), kjo e fundit zvogëlohet dhe tretësira zbardhet. Karakterizohet nga një reagim i kthyeshëm dhe i ngadaltë i ndërveprimit me alkoolet (esterifikimi), si rezultat i të cilit formohen esteret: HOOC - COOH + 2HOR ↔ 2H2O + ROOC - COOR.
Në industri, acidi oksalik merret nga oksidimi i përbërjeve kimike. Për shembull, në prani të një katalizatori vanadium (V2O5), alkoolet, karbohidratet dhe glikollat \u200b\u200boksidohen me një përzierje të acideve nitrik (HNO3) dhe sulfurik (H2SO4). Përdoret gjithashtu metoda e oksidimit të etilenit dhe acetilenit (HNO3) në prani të kripërave të paladiumit Pd (NO3) 2 ose PdCl2. Acidi oksalik merret nga propileni, i cili oksidohet me dioksid azoti të lëngshëm (NO2). Metoda e prodhimit të acidit nga bashkëveprimi i hidroksidit të natriumit (NaOH) me monoksidin e karbonit (CO) përmes fazës së ndërmjetme të formimit të NaOH + CO → HCOONa ka perspektiva të mira. Pastaj formohet oksalat natriumi dhe hidrogjeni evoluohet: HCOONa + NaOH → NaOOC - COONa + H2. Acidi oksalik merret nga oksalati i natriumit në një mjedis acid: NaOOC - COONa + 2H + → HOOC - COOH + 2Na +.
Acidi oksalik dhe oksalatet janë të pranishme në shumë bimë, përfshirë çajin e zi, dhe gjenden te kafshët. Dëmi kryesor për njerëzit shoqërohet me insuficiencë renale, e cila ndodh për shkak të ndërveprimit të acidit oksalik me kalcium, si rezultat, ndodh reshje e ngurtë (CaC2O4) - përbërësi kryesor i gurëve në veshka. Acidi provokon dhimbje në nyje për shkak të depozitimit të përbërjeve të tilla në to. Acidi oksalik mund të prodhohet në trup përmes metabolizmit të etilen glikolit nga mjedisi (p.sh., pistës së aeroportit dhe agjentit të shkrirjes së aeroplanit dhe burimeve të tjera antropogjene). Problemet e mundshme me oksalatin te njerëzit mund të ndahen në dy. Së pari, një kalcium i rëndësishëm makroelement është i lidhur nga acidi oksalik dhe mungesa e tij formohet në qelizat e indeve dhe organeve. E dyta është formimi i gurëve në veshka. Sasia më e madhe e acidit oksalik gjendet te spinaqi, gjethet dhe kërcelli i ravenit, lëpjeta, panxhari, majdanozi dhe qepët e njoma.
- përfaqëson kristale higroskopike monoklinike të pangjyrë, të tretshëm në ujë, në një masë të kufizuar në alkool etilik dhe eter dietil, të patretshëm në kloroform, eter naftë dhe benzinë.Acidi oksalik është një kufi dibazik acid karboksilik... Bën pjesë në acide të forta organike. Ka të gjitha vetitë kimike të acideve karboksilike. Kripërat dhe esteret e acidit oksalik quhen oksalate. Acidi oksalik formon estere acide dhe të mesme, amide, klorid acid.
Në natyrë, ajo gjendet në lëpjetë, raven dhe disa bimë të tjera në formë të lirë dhe në formën e oksalateve të kaliumit dhe kalciumit.
Dendësia 1.36 g / cm³. Pika e shkrirjes - 189.5 ° C, temperatura e lartësimit - 125 ° C, temperatura e zbërthimit - 100-130 ° C, temperatura e dekarboksilimit - 166-180 ° C.
Formula kimike: C 2 H 2 O 4
 Përdorimi i acidit oksalik.
Përdorimi i acidit oksalik.
- në industrinë kimike (sinteza organike, në prodhimin e plastikës, bojës, në sintezën e ngjyrave, si përbërës i përbërjeve piroteknike);
- në metalurgjinë kimike (si një përbërës i përbërjeve për pastrimin e metaleve nga ndryshku, shkalla, oksidet); - në kiminë analitike (si një precipitant i elementeve të rralla të tokës);
- në mikroskopi (si një agjent zbardhues për feta);
- në industrinë e tekstilit dhe lëkurës (e përhapur në shtypjen e pambukut dhe kur ngjyroset leshi dhe mëndafshi, kur nxihet lëkura);
- në prodhimin e detergjenteve sintetikë (si zbardhues dhe dezinfektues, mjete për pastrimin dhe largimin e gurëve urinarë, kripërave të fortësisë dhe ndryshkut);
- në kozmetikë (si një shtesë aktive në zbardhjen dhe kremrat e njollave);
- në sistemet e pastrimit të ujit (metoda kimike e pastrimit dhe zvogëlimit të fortësisë së ujit, pastrimi i bartësve të nxehtësisë në termocentralet bërthamore);
- në mjekësi dhe farmaceutikë.
Kërkesat e sigurisë
Acidi oksalik është një substancë e djegshme, në gjendjen e vendosur, pluhuri i acidit oksalik është i rrezikshëm nga zjarri, sipas shkallës së ndikimit në trup, i përket substancave të klasës së 2-të të rrezikut.
Ka një efekt irritues të fortë në lëkurë, mukozën e syve dhe traktin e sipërm respirator. Acidi oksalik dhe kripërat e tij janë toksikë. PPE duhet të përdoret kur punoni me acid oksalik.
Paketimi, transportimi dhe magazinimi.
Acidi oksalik teknik është i paketuar në qese polietileni ose qese të bëra me film polietileni me shtypje me ngjyra. Mund të paketohet në bateri kompensatë me një mbështjellës filmi ose kontejnerë të butë të specializuar për përdorim të vetëm.
Acidi oksalik transportohet nga të gjitha llojet e transportit. Ruani në paketimin e prodhuesit në depo të mbyllura, të ajrosura në paleta.
Afati i ruajtjes së garantuar është 6 muaj nga data e prodhimit.
(ethavdiic) është një acid karboksilik i ngopur dibazik, i cili është një substancë kimike në formën e kristaleve pa ngjyrë, e tretshme në ujë, jo plotësisht në alkool dietil dhe etil, i patretshëm në benzinë, kloroform, eter naftë. Esteret dhe kripërat e këtij acidi quhen oksalate. Ky kimikat është një acid i fortë organik me një pikë shkrirje -189.5 ° C. Në natyrë, kjo përbërje kimike në formë të lirë, si dhe në formën e oksalateve (estereve dhe kripërave të acidit oksalik) të kaliumit dhe kalciumit gjendet në shumë bimë: raven, fasulet, spinaqi, arrat, soja. Ky acid formohet gjatë fermentimit oksalik. Për herë të parë, ky lloj acidi u mor gjatë sintezës së cianogjenit nga kimisti Friedrich Wöhler (Gjermani, 1824).
Zbatimi i acidit oksalik
Si çdo acid, oksalik për shkak të tij vetitë unike të përdorura në industritë e mëposhtme:
- kimike (në prodhimin e plastikës, ngjyrave, bojës, piroteknikës);
- metalurgjik (për pastrimin e metaleve nga korrozioni, oksidet, shkallët, ndryshku);
- tekstil dhe lëkurë (si ngjyrues, kur ngjyrosni mëndafshin dhe leshin);
- bletari (për përpunimin e bletëve);
- kimikate shtëpiake (të përfshira në shumë detergjentë dhe pluhura si zbardhues dhe dezinfektues);
- kimi analitike (precipitues i elementeve të rralla të tokës);
- mikroskopi (feta zbardhues);
- kozmetologji (përbërës zbardhues për njolla);
- mjekësi dhe farmakologji;
- Njoftime
Rëndësia e acidit oksalik për trupin
Kjo përbërje kimike në trupin e njeriut është një produkt i ndërmjetëm që excretohet në urinë si kripëra kalciumi. Në shkelje të metabolizmit të mineraleve, kripërat e këtij acidi marrin pjesë në formimin e gurëve në fshikëzën dhe veshkat. Ky acid organik që gjendet në perimet e papërpunuara është shumë i dobishëm për trupin tonë. Kombinohet lehtësisht me kalciumin dhe promovon thithjen e tij. Acidi oksalik në perimet e ziera është i dëmshëm për shëndetin pasi bëhet joorganik. Kjo çon në lidhjen e kalciumit, dhe si rezultat - në mungesën e tij në indet e eshtrave, e cila është shkaku i dëmtimit të tij. Sekretimi ditor i acidit oksalik së bashku me urinën tek një i rritur është 20 mg, tek fëmijët deri në 1.29 mg / kg.
Masat paraprake
 Acidi oksalik i përket reagentëve kimikë të ndezshëm, shumë toksikë dhe toksikë, prandaj, vetëm ata punonjës të laboratorit që kanë kaluar nëpër udhëzime të veçanta për respektimin e masave të sigurisë lejohen të punojnë me të:
Acidi oksalik i përket reagentëve kimikë të ndezshëm, shumë toksikë dhe toksikë, prandaj, vetëm ata punonjës të laboratorit që kanë kaluar nëpër udhëzime të veçanta për respektimin e masave të sigurisë lejohen të punojnë me të:
- të kryejë punë në qelqe të veçanta laboratorike. Nëse qelqet laboratorike janë bërë nga një material tjetër, acidi mund të reagojë me të;
- në mënyrë që të shmanget hyrja e acidit oksalik në lëkurë, traktin respirator, në mukozën, të gjitha studimet duhet të kryhen: në produkte gome (çizme, kalata të gomuara, doreza ekzaminimi, doreza nitrile), pajisje mbrojtëse (maskë gazi ose aparat respirator, syze), tuta;
- ndërsa përdorni acid oksalik, është e ndaluar të hani, të pini, të pini duhan;
- pas përfundimit të punës, është e nevojshme të lani plotësisht fytyrën dhe duart me ujë të ngrohtë dhe sapun ose një agjent neutralizues (tretësirë \u200b\u200bsode buke);
- është e ndaluar të transportohet dhe ruhet acidi oksalik së bashku me të ushqim;
- vëzhgoni masat e sigurisë nga zjarri nëse ka nevojë të përdorni pajisje ngrohëse.
Ju duhet të dini se acidi oksalik i përket acideve të forta organike, përdorimi i tij në një numër i madh mund të shkaktojë acarim të ezofagut, zorrëve, stomakut, lëkurës dhe traktit respirator. Nëse kjo kimike hyn në trup, mund të shfaqet një ndjesi djegieje, të vjella me gjak. Ndihma e parë në situata të tilla është shpëlarja e zonës së prekur të lëkurës me shumë ujë. Ruani acidin në një qese plastike të mbyllur në një zonë të ajrosur mirë në paleta.
Blini acid oksalik
Blini acid oksalik, blini acid borik, acid citrik ju mund të blini, blini acid laktik, si çdo reagjent tjetër kimik, në dyqanin e reagentëve kimikë Moska me pakicë dhe shumicë "Prime Chemicals Group". Faqja jonë ka gjithçka që i duhet një laboratori modern shkencor ose industrial. Blerja e ndonjë produkti në dyqanin tonë në internet, ju blini një produkt me një certifikatë cilësie që plotëson të gjitha standardet e GOST me çmime të volitshme dhe përjashton mundësinë e blerjes së një false.
"Prime Chemicals Group" është një garanci e cilësisë së produkteve të ofruara.
Ju mund të blini acid oksalik me shpërndarje në qytet dhe rajon Fitim!
Acidi oksalik (etanedioik) është një përbërje karboksilike dibazike që i përket klasës së acideve të forta organike.
 Substanca është e përhapur në natyrë, gjendet në formën e kripërave, eterëve, amideve, izomereve të lira. Burimet kryesore të acidit oksalik janë raven e freskët, spinaqi, lëpjeta, panxhari i gjetheve. Këto produkte "furnizojnë" trupin dhe janë të domosdoshëm për hematopoiezën, si dhe stimulojnë zorrët.
Substanca është e përhapur në natyrë, gjendet në formën e kripërave, eterëve, amideve, izomereve të lira. Burimet kryesore të acidit oksalik janë raven e freskët, spinaqi, lëpjeta, panxhari i gjetheve. Këto produkte "furnizojnë" trupin dhe janë të domosdoshëm për hematopoiezën, si dhe stimulojnë zorrët.
Për herë të parë acidi etanedioik u sintetizua nga cianogjeni në 1824 nga biokimisti gjerman Friedrich Wöhler. Në një shkallë industriale, ajo merret duke oksiduar sheqerin me acid nitrik në prani të një katalizatori për reagimin e pentoksidit të vanadiumit. Në formën e oksalatit të kalciumit, përbërja gjendet në të gjitha bimët.
Ndikimi në trupin e njeriut
Acidi oksalik është i përfshirë në metabolizmin thelbësor, dhe gjithashtu ka një efekt baktervrasës në traktin tretës.
Kërkesa ditore për substancën është 20 - 30 miligramë. Niveli i sipërm i lejueshëm i marrjes së acidit është 50 miligramë, tejkalimi i këtij pragu çon në zhvillimin e simptomave të mbidozës në trup.
![]() Përbërja e karbonit përdoret për patologjitë e mëposhtme:
Përbërja e karbonit përdoret për patologjitë e mëposhtme:
- infertilitetit;
- dhimbje koke (migrenë);
- menopauza atipike;
- amenorrea;
- pushtimet helmintike;
- gjakderdhje;
- tuberkulozi kronik;
- impotencë;
- sinusit, sinusit;
- zorrët e ngadalta;
- dhimbje reumatike;
- periudha të dhimbshme me gjakderdhje të bollshme;
- trikomoniaza, klamidia;
- infeksione të zorrëve (Staphylococcus aureus, Escherichia coli, kolera, ethe tifoide).
Mos harroni, marrja e tepërt e ushqimit oksalik çon në përthithjen e dëmtuar të kalciumit. Si rezultat, gurët oksalate formohen në organet gjenitourinar. Në të njëjtën kohë, kristalet e dëmshëm "shkojnë" përgjatë kanaleve urinare, duke dëmtuar mukozën dhe duke u ngjyrosur me ngjyrë të zezë me pigmentin e gjakut. Si rezultat, një person ka dhimbje të mprehta në zgavrën e barkut, ijë dhe mbrapa, është e vështirë të urinosh, ngjyra e urinës ndryshon.
Marrja e sasive të mëdha të acidit, përveç formimit të gurit, shkakton problemet e mëposhtme:
- dobësi;
- të përziera;
- mërzitje në stomak;
- marramendje;
- ndjesi djegieje në sinuse, gojë, fyt;
- ngërçet në bark.
Në raste të rënda, frymëmarrja bëhet e vështirë dhe shfaqet dhimbja e gjoksit.
Përveç kësaj, mbajtja e acidit etanedioik në trup mund të jetë rezultat i çrregullimeve nervore. Për të stabilizuar ekuilibrin acid-bazë, përveç uljes së konsumit të produkteve oksalike, ato marrin komplekse qetësuese. Nëse nuk ishte e mundur të ndaloni simptomat e tepërta vetë, duhet menjëherë të kontaktoni një gastroenterolog.
Aplikacion
 Për shkak të vetive të tij baktervrasëse dhe zbardhuese, acidi oksalik përdoret me sukses në industritë e mëposhtme:
Për shkak të vetive të tij baktervrasëse dhe zbardhuese, acidi oksalik përdoret me sukses në industritë e mëposhtme:
- metalurgjik (për pastrimin e metaleve nga shkalla, korrozioni, ndryshku, oksidet);
- kimike (në prodhimin e ngjyrave, plastikës, bojës, piroteknikës);
- tekstil (si i paqëndrueshëm kur ngjyroset leshi dhe mëndafshi);
- mikroskopi (për zbardhjen e seksioneve);
- bujqësia (si insekticid);
- farmakologji;
- punime druri;
- kozmetologji (si pjesë e kremrave, maskave dhe serumeve zbardhuese);
- kimia analitike (për reshjet e elementeve të rralla të tokës);
- kimikate shtëpiake (si përbërës zbardhues dhe dezinfektues i detergjenteve).
Përveç kësaj, substanca përdoret për të krijuar aditivët e ushqimit dhe komplekset biologjikisht aktive (si ruajtës).
Masat paraprake
Acidi oksalik i përdorur në industri i përket reagjentëve shumë toksikë të klasës së tretë të rrezikut. Prandaj, kur punoni me të, është e rëndësishme të vëzhgoni masat paraprake të sigurisë.
![]() Masat paraprake:
Masat paraprake:
- Kryeni çdo hulumtim në veshjet prej gome (çizme, doreza, përparëse) dhe pajisje mbrojtëse (aparate për frymëmarrje ose gaz, syze). Pajtueshmëria me këtë kërkesë do të ndihmojë për të shmangur marrjen e acidit etanedioik në lëkurë, mukozat e fytyrës, në traktin respirator.
- Kryeni punë në enë qelqi. Nëse pajisjet laboratorike janë bërë nga një material tjetër, acidi mund të reagojë me të.
- Në procesin e përdorimit të substancës, është rreptësisht e ndaluar të pini, të pini duhan, të hani.
- Pas mbarimit të punës me përbërësin, lani fytyrën dhe duart plotësisht me sapun dhe ujë.
- Transportimi i përbashkët i acidit dhe ushqimit është rreptësisht i ndaluar.
- Nëse është e nevojshme të përdorni pajisje ngrohëse, vëzhgoni teknikat e sigurisë nga zjarri.
- Ruani përbërësin në një enë plastike të mbyllur në paleta në një zonë të ajrosur.
Nëse acidi teknik futet në lëkurë, mbulesa e prekur lahet me ujë, dhe nëse është e nevojshme, kërkoni ndihmë mjekësore.
Burimet natyrore
Magazinimi i acidit etanedioik është produkt origjina bimore: përqendrimi i substancës në gjethet e bimëve është shumë më i lartë se në kërcell dhe rrënjë.
| Emri i produktit | Përmbajtja e substancës karbonike për 100 gram ushqim, miligram |
|---|---|
| Lëpjetë | 700 — 850 |
| Raven | 850 |
| Spinaq | 600 – 750 |
| Panxhar fletë (chard) | 500 — 670 |
| Asparagus | 640 |
| Fasule kakao | 550 — 600 |
| Panxhar | 500 |
| Kokrra gruri të mbirë | 270 |
| Kikirikë të pjekur | 180 |
| Çokollate e zezë | 110 |
| Majdanoz | 100 |
| Lëvore limoni, gëlqere | 90 |
| Presh | 85 |
| Rrush | 26 |
| Selino | 20 |
| Rrush pa fara e kuqe | 19 |
| Patëllxhan | 18 |
| luleshtrydhe | 16 |
| Bizele jeshile (te fresketa) | 15 |
| Mjedra | 14 |
| Mbjellja e majdanozit | 11 |
| Kumbull | 10 |
| Kumbulla të thata | 6 |
| Bizele me sy te zi | 5,5 |
| Pjeshkat | 5 |
| Rrush pa fara e zezë | 4,5 |
| bukë e bardhë | 4,5 |
| Çaj i zi | 4,5 |
| Portokall | 4 |
| Karrota | 4 |
| Mollë, dardha | 3 |
| Domate | 2 |
| Qershi | 1,5 |
| Kastravecat | 1 |
Acidi oksalik është i pranishëm në sasi të vogla (0,3 - 2 miligramë) në të gjitha produktet e qumështit, mishit dhe peshkut.
Interesante, në proces trajtimit të ngrohjes produktet, substanca kalon në një formë inorganike, duke formuar kripëra të tretshme me pak kalcium (oksalate). Konsumi i rregullt i ushqimit të tillë, përveç formimit të gurit, çon në thithjen e dëmtuar të kalciumit, dhe si rezultat, shkatërrimin e indit të kockave dhe kërcit.
Acidi etanedioik - ilaç efektiv lufta kundër bletëve të mbartura nga rriqrat (varroatoza, akarapidoza).
Pushtimi eliminohet me spërkatje të shpërndarë imët të insekteve me tretësirë \u200b\u200boksalike. Për ta bërë këtë, 20 gramë acid teknik treten në një litër ujë të ngrohtë jo të fortë (merret një insekticid ujor dy përqind). Përbërja përgatitet menjëherë para përdorimit.
Për të vulosur bletët, huallët dhe huallët e bletëve hiqen nga zgjua. Pas kësaj, kornizat me insekte nxirren nga ana tjetër, duke i spërkatur ato në të dy anët. Për përpunimin e një strukture, konsumohen 10 - 12 mililitra tretësirë.
Në rastin e përdorimit të avujve të acidit oksalik, dhoma e sipërme mbyllet në zgjua dhe 10-14 re tymi futen në atë të poshtme. Pastaj 2 gramë të substancës derdhen në dhomëzën e punës (për çdo 10-15 korniza me pllaka), duke ngrohur tubin e daljes me një furrë (5 - 6 sekonda). Pas kësaj, ngrohësi futet në vrimë çezme për 30-40 sekonda, duke pritur shfaqjen e smogut nga provat e "duhanpirësit". Pas përfundimit të gdhendjes, ajri pompohet në dhomë duke përdorur një pompë automobilistike (4 - 7 goditje të plota).
Trajtimi i përbërjes oksalike kryhet 2 - 5 herë në vit. Shtë e këshillueshme që të përdorni një tretësirë \u200b\u200bujore në një temperaturë ambienti prej të paktën 16 gradë dhe avujt e acidit të paktën 10 gradë. Përpunimi primar i koshereve kryhet në fillim të pranverës, pas një fluturimi masiv të bletëve. Me një pushtim të fortë, procedura përsëritet pas 7 deri në 12 ditë. Përpunimi sekondar i bletëve kryhet në verë, pas pompimit të mjaltit komercial dhe para ushqimit të insekteve. Nëse ka nevojë për veshje vjeshte, procedura kryhet pasi "punëtorët" të lënë pjellën.
Produkti
Pra, acidi oksalik është një përbërje natyrore që gjendet në produktet bimore. Substanca promovon hematopoezën e duhur, përshpejtimin e metabolizmit, "dezinfektimin" e traktit tretës. Burimet kryesore të acidit etanedioik janë lëpjetë, spinaqi, raven, dhe fisi i Zvicrës. Niveli optimal i konsumit të elementit është 20 - 30 miligramë në ditë. Sidoqoftë, është e rëndësishme të merret në konsideratë se një tepricë e acidit në trup është e mbushur me formimin e gurëve oksalate në organet gjenitourinar. Prandaj, këshillohet që njerëzit me sëmundje të veshkave, artrit reumatoid, diabet të acidit urik dhe përdhes të kufizojnë marrjen e kësaj lënde.